Phanta Super-Fidelity DNA Polymerase
扩增能力强的高保真酶,让科研更加顺利!

菌落PCR;分子克隆;高GC体系;基因鉴定

高保真度:保真度是Taq DNA Polymerase的52倍
扩增速度快:扩增速度可达15 - 30 sec/kb
模板适应性广:广泛适用于各种类型模板
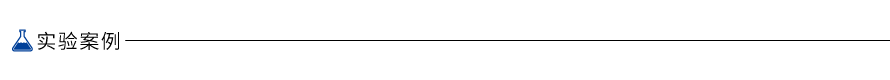
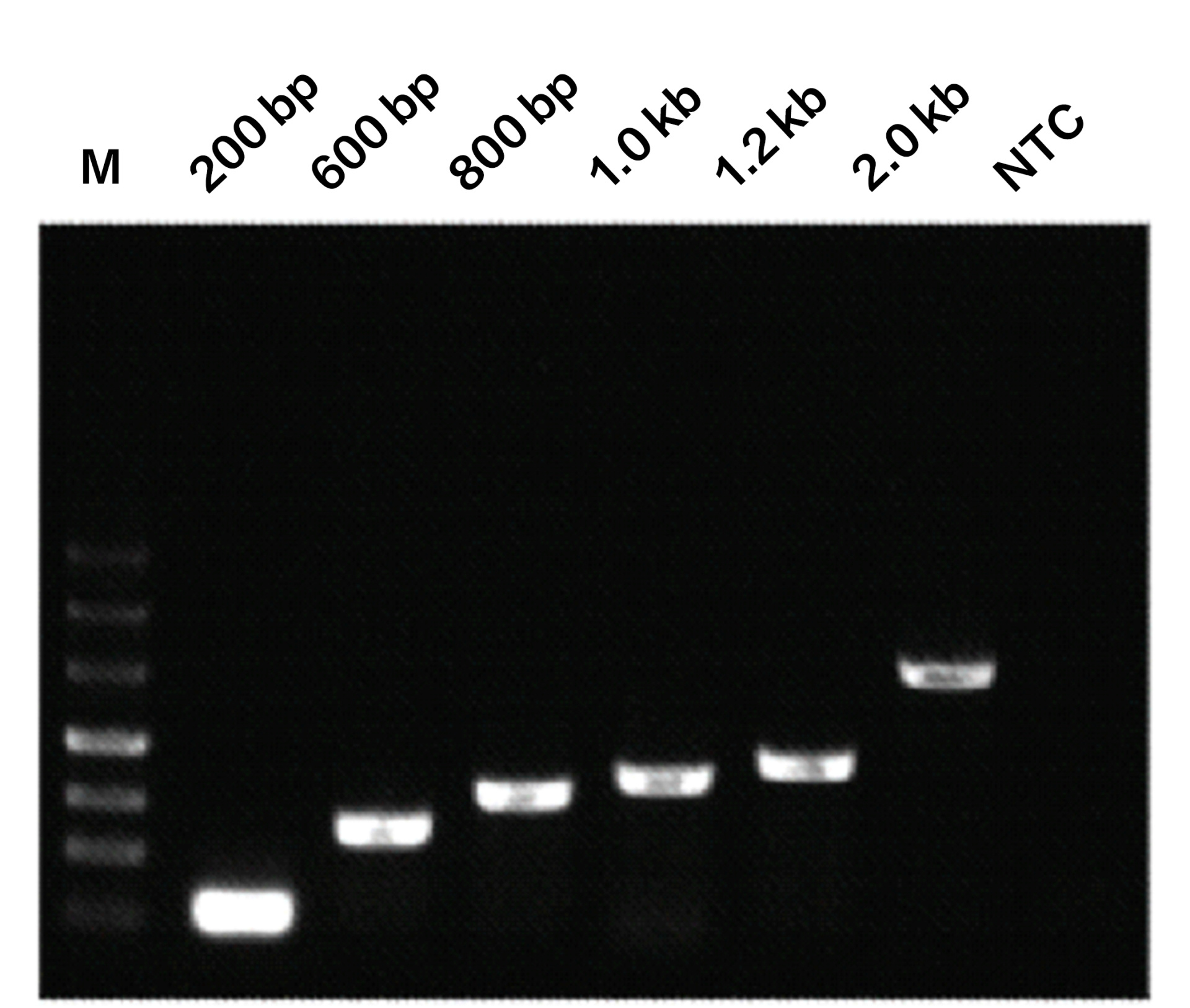
图1
使用Phanta Super-Fidelity DNA Polymerase以λ DNA为模板扩增长度分别为200 bp、600 bp、800 bp、1 kb、1.2 kb、2.0 kb的目标片段,延伸时间设置为1秒。所有片段均可以实现特异性高产量扩增。
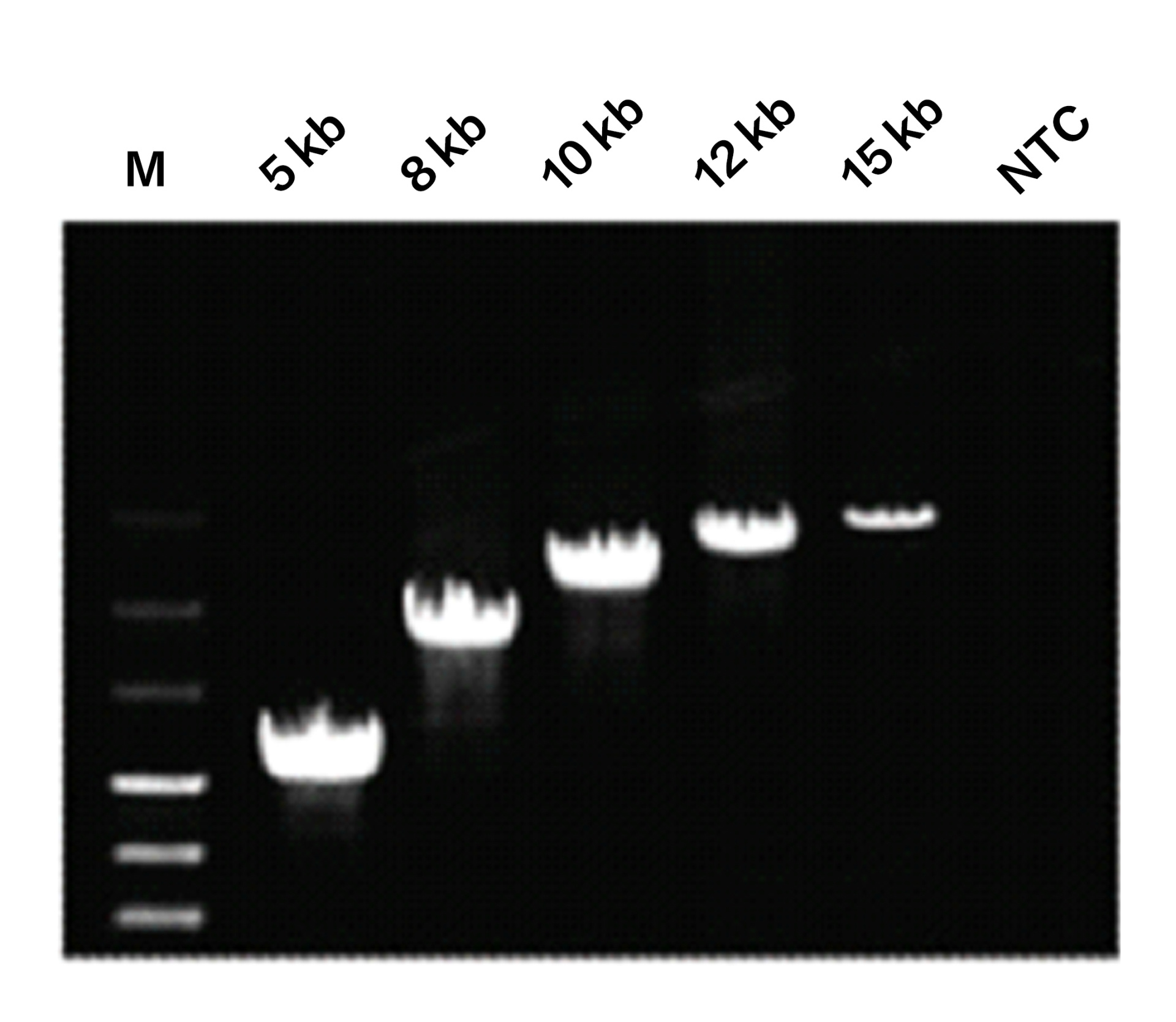
图2
使用Phanta Super-Fidelity DNA Polymerase以λ DNA为模板扩增长度分别为5 kb、8 kb、10 kb、12 kb、15 kb的目标片段,延伸时间设置为3分钟。所有片段均可以实现特异性高产量扩增。
图3
使用LacI法测定,Phanta保真性是普通Taq DNA聚合酶的52倍,是野生型Pfu DNA聚合酶的6倍。
(Cline et al. , Nucleic Acids Research,24: 3546-3551(1996))

本产品是一种基于对Pfu DNA Polymerase的基因工程改造而成的新一代超保真DNA聚合酶,具有较高的扩增效率和广泛的模板适应性。5 × Phanta SF反应缓冲液对于简单或复杂模板、短片段或长片段PCR扩增均具有良好的适应性,附带的PCR Enhancer可有助于高GC含量片段的扩增。该酶具有5'→3'聚合酶活性和3'→5'外切酶活性,扩增产物为平端,适用于ClonExpress和拓扑克隆试剂盒(Vazyme #C112/C113/C115/C601)。


-20°C保存
Q1:扩增效率低,实验组无扩增条带。
A1:(1) 引物
检查人工合成的引物是否因存储条件不当而降解;引物设计是否合理,可利用BLAST检查引物特异性或重新设计引物。
(2) 模板
长期放置、反复冻融会导致模板断裂、开环或降解,应使用新鲜制备的DNA双链作为模板;模板GC含量过高会导致DNA的双链无法打开,此时加入PCR Enhancer(货号P021),可以有效降低解链温度;模板的AT含量过高,可尝试使用针对高AT的产品(货号P501/P511);模板为粗品,存在抑制物,建议降低模板浓度(稀释使用;若样本为植物叶片,要确保植物为非多糖多酚植物,取新鲜幼嫩的叶片,并将叶片面积剪小,如黄枪头尖部面积大小);若模板为cDNA,要确认逆转录所用RNA的纯度及完整度。
(3) 酶
反应所用的酶失活,建议更换新酶或用另一来源的酶重新实验。
(4) 扩增体系
反应体系配制错误,建议重复实验。
(5) 反应程序
检查变性温度是否准确,PCR仪指示温度与实际温度是否相符,如果温度过高,酶在前几个循环就迅速失活,温度过低则模板变性不彻底;若模板为酵母菌,可将预变性时间延长10min;退火温度不合适,可对退火温度设置梯度,摸索合适的退火温度;如果目的片段较长,可尝试Touch Down 程序;检查延伸时间是否充足。
(6) Mg2+浓度不合适
Mg2+浓度过低可影响PCR产量甚至使PCR扩增失败;Mg2+浓度过高会降低PCR的特异性,应适当调整Mg2+浓度。
Q2:扩增的条带亮度不太亮。
A2:(1) 引物
检查引物是否降解。
(2) 模板
首先确认模板的质量,长期放置、反复冻融会导致模板断裂、开环或降解,应使用新鲜制备的DNA双链作为模板;如果模板没有了,可用首次扩增产物按倍比稀释后作为模板进行二次扩增。
(3) 酶
可适当提高酶的使用量。
(4) 反应程序
可尝试使用Touch Down程序;延长延伸时间,提高循环数。
Q3:扩增特异性差,非特异性扩增。
A3:(1) 引物
引物设计不够优化。引物与靶序列有非特异性互补或自身聚合成二聚体,可降低引物浓度进行优化,必要时重新设计引物。
(2) 模板
模板不纯,被污染,需重新制备模板。
模板降解或过量,通过电泳检查模板完整性及浓度,必要时重新纯化模板。模板的使用量请参考说明书。
(3) 反应程序
反应程序不够优化。如果出现比目的条带小的杂带,可通过提高退火温度,降低循环数调整;如果出现比目的条带大的杂带,可缩短延伸时间、降低循环数。
(4) 酶
酶量加入过多。高保真系列:50μl体系加1U。
Q4:扩增产物跑胶条带弥散或拖尾。
A4:(1) 胶
制胶时要使胶完全融化。
(2) 引物
检查人工合成的引物是否因存储条件不当而降解。
(3) 模板
模板降解或过量,可通过电泳检查模板完整性及浓度,必要时重新制备模板。模板的使用量请参考说明书。如果目的条带较长,模板是cDNA,要确认逆转录所用RNA的纯度及完整度,逆转录时不加随机引物重新逆转录。
(4) 反应程序
反应程序不够优化。退火温度不合适,可对退火温度设置梯度,摸索合适的退火温度;尝试Touch Down 程序。
(5) 酶
酶量加入过多。高保真系列:50μl体系加1U。
Q5:空白对照出现扩增产物。
A5:(1) 引物设计不合理
扩增序列与非目的扩增序列有同源性,PCR也可以扩增出非靶序列的序列。
(2) 若扩增产物条带大小与目的条带一致,说明有污染
更换新的Mix、水或引物重复实验。反应体系在超净工作台内配制,减少气溶胶污染。
(3) 为了避免靶序列受到整个基因组或大片段的交叉污染,操作时应小心轻柔,防止将靶序列吸入加样枪内或溅出离心管外。
(4) 为了避免靶基因受到空气中小片段核酸污染,可用巢式PCR方法减轻或消除污染。
Q6:高保真酶扩增保真性差,存在突变。
A6:高保真酶在PCR时扩增产物有突变,可以从以下几点来分析:
(1) 模板本身存在突变
检查模板,若模板是质粒,建议送质粒去测序;若模板是cDNA,建议重复实验,如果仍有突变,可能是cDNA有问题,建议重新制备cDNA,制备cDNA前检测RNA的完整度及纯度。
(2) 模板长时间在紫外光下照射,引入突变
切胶回收过程中避免长时间在紫外光下照射。
(3) 基因序列与NCBI上的不一致
建议再重复一次送去测序,若结果和上一次一样,说明序列可能和NCBI上的不一致。
(4) 少量序列存在非严谨序列
有相似重组序列,导致重组错位。
Q7:逆转录后的产物cDNA作为模板,高保真酶,一次应该加多少体积?
A7:说明书建议cDNA模板使用量为1-5μl(不超过PCR反应总体积的1/10),可在这个范围内尝试不同的使用量,摸索合适使用量。
Q8:高保真酶扩增产物是否带A尾,如何加A尾
A8:(1)高保真酶扩增产物不带A,后续做克隆可尝试使用Vazyme无缝克隆产品C601;若进行TA克隆可用普通的Taq酶进行加A尾;

相关产品
GR501-01/02
MD102-01/02
FastPure Gel DNA Extraction Mini Kit
DC301-01
ClonExpress Ultra One Step Cloning Kit
C115-01/02
C502-02/03




